A química depende dos laços e afinidade de seus componentes para produzir o mundo e tudo o que conhecemos nele. Essas ligações químicas não são apenas desejadas, mas sim, necessárias para haver estabilidade atômica. Todos querem um pouco de sossego em sua existência.
Uma boa parcela dos elementos da Tabela Periódica alcançam esse status de equilíbrio ao obterem oito elétrons em sua última camada de valência, isso é chamado de regra do octeto. Porém, alguns são menos exigentes e não precisam de tudo isso para se manterem estáveis, como o hélio, berílio, hidrogênio, alumínio, lítio e claro, a estrela do dia: o boro.
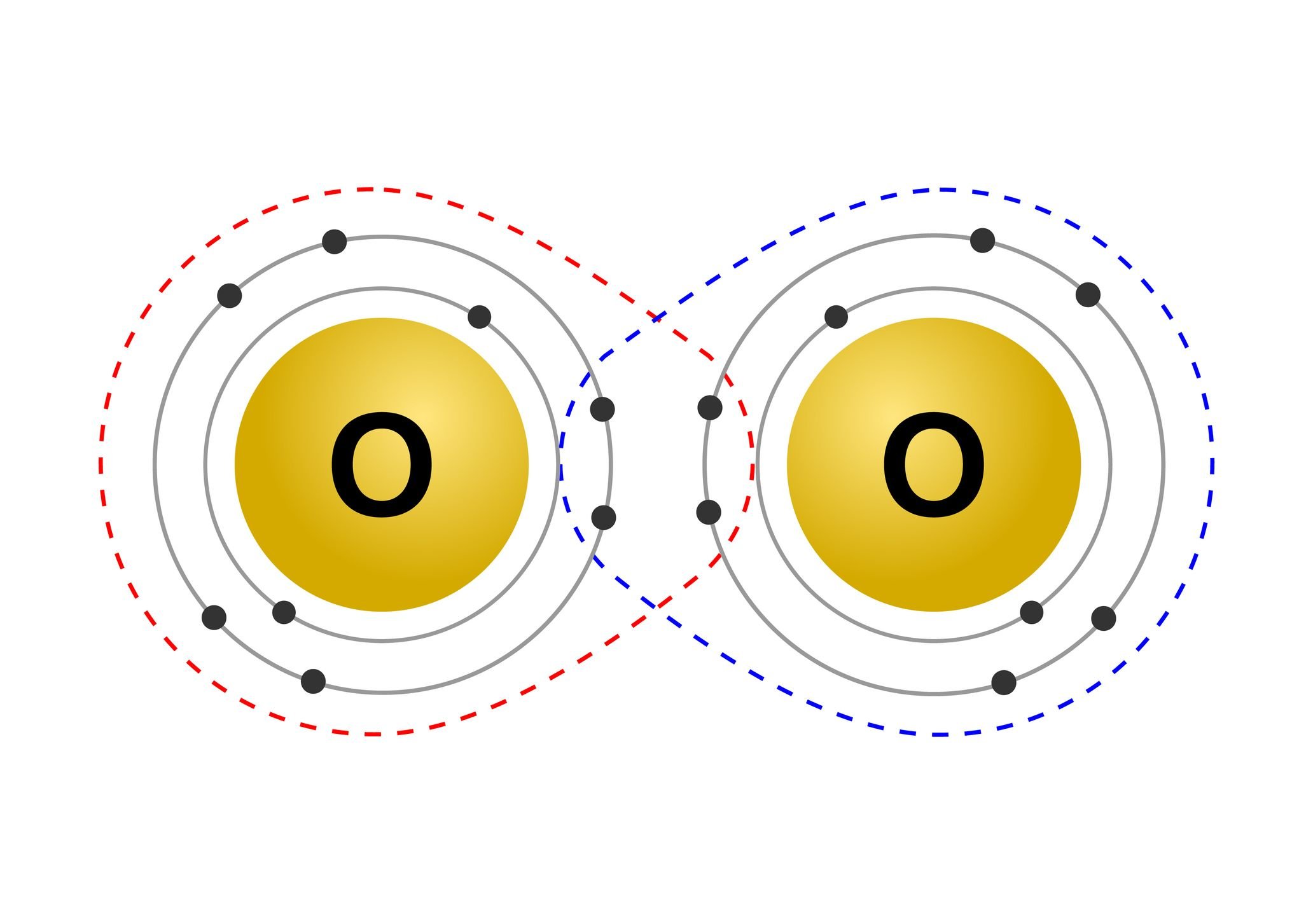
Como nem tudo se compra no mercado ou na internet, para obter elétrons, os elementos precisam ligar-se reciprocamente, seja de uma maneira altruísta que irá doar elétrons ou através do compartilhamento.
Mas assim como ocorre no macro, em términos desastrosos, o rompimento dessas ligações podem gerar núcleos partidos e explosões muito úteis para produção de energia.
E a nova descoberta dos pesquisadores da Universidade de Würzburg, Alemanha, pode nos dar uma ligação a mais para romper e produzir coisas interessantes. Não que estejamos interessados em términos bombásticos.
Os laços que unem o mundo: ligações químicas
As ligações químicas são a maneira como os átomos constroem os seres vivos e o mundo. Elas podem ocorrer de maneiras diferentes, com a ‘doação’ ou compartilhamento de elétrons. As principais ligações são chamadas de Ligações Iônicas e Covalentes.
Nas ligações iônicas, existe um átomo doador e um receptor. Quando há essa transferência de elétrons a polaridade dos átomos pode se inverter, assim, os núcleos se atraem formando a molécula.
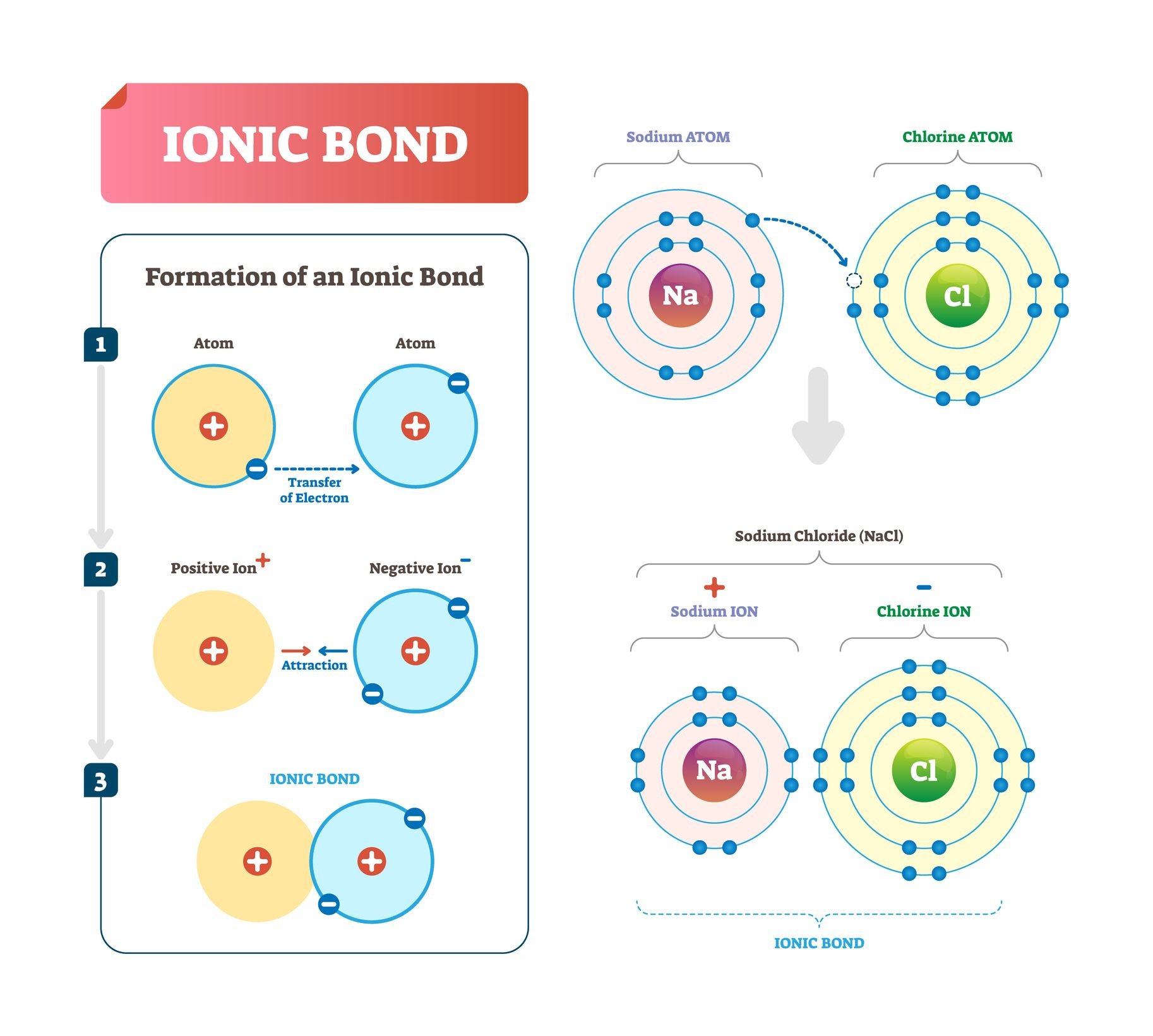
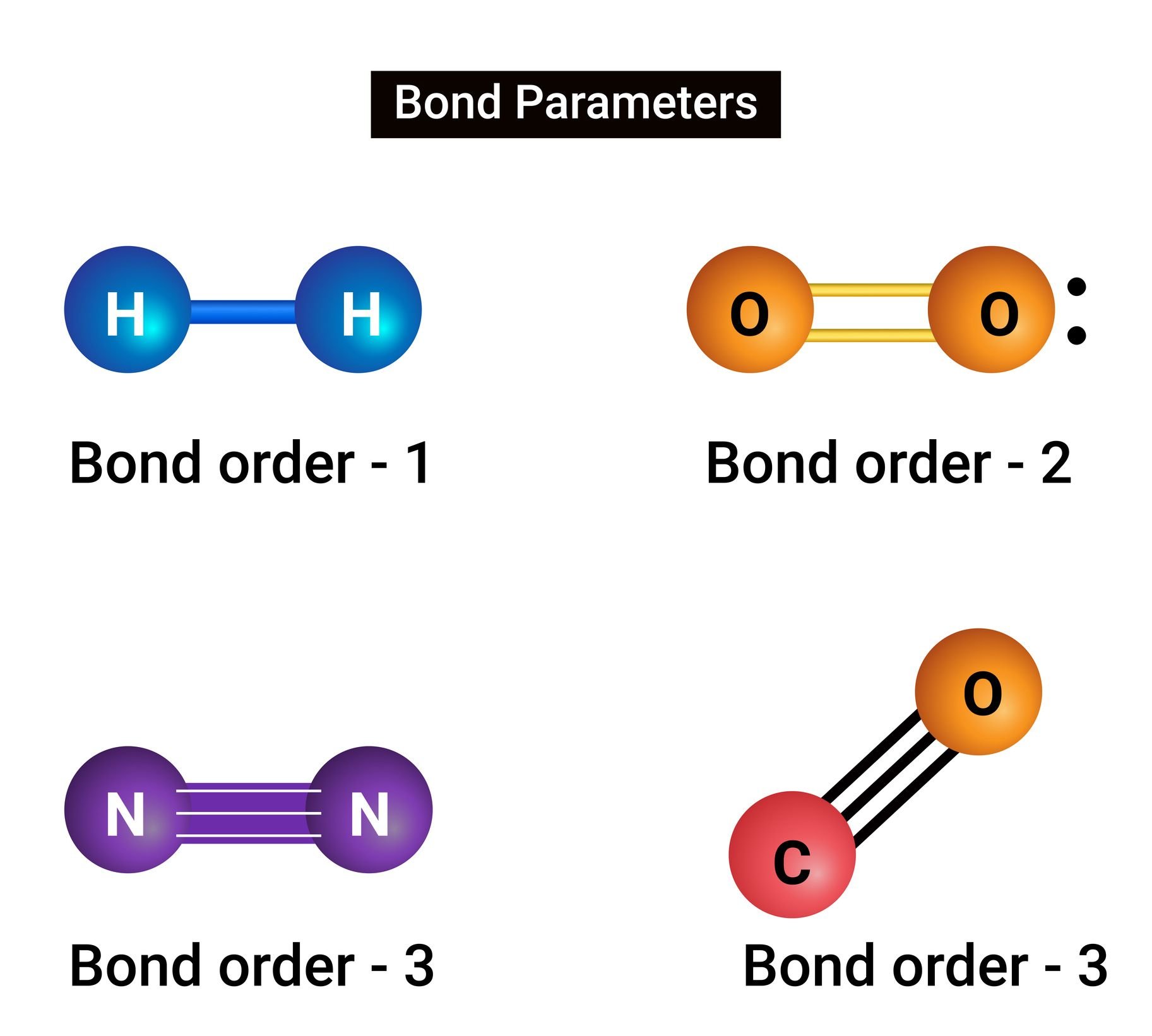
Entretanto, se doar não é uma possibilidade, as ligações podem ser produzidas pelo compartilhamento de elétrons. Nas ligações covalentes, mais de um par de elétrons pode ser associado, assim, as ligações podem ser simples, duplas, triplas ou dativas.
Esse uso conjunto dos elétrons da última camada de valência irá depender da necessidade que cada núcleo possui para atingir sua estabilidade eletrônica, então, nem todos os elementos irão ser capazes, ou possuir a necessidade de produzir mais de uma ligação. Mas há um grupo que costuma construir ligações triplas entre si.
O Oxigênio, Nitrogênio, Boro e Carbono são conhecidos por produzir moléculas com ligações triplas entre si. Contudo, mesmo que possuam maior susceptibilidade, alguns desses arranjos ainda não haviam sido observados, como no caso do Boro e do Carbono. Mas isso era passado.
Boro-Carbono ou Borino para os íntimos
Pela primeira vez, pesquisadores da Universidade Julius-Maximilians Würzburg na Baviera, Alemanha, produziram uma molécula com tripla ligação entre Carbono e Boro. Moléculas com ligações duplas já eram conhecidas e não são incomuns. A pesquisa foi publicada no periódico Nature Synthesis.
Para produzir o feito, o grupo “aprisionou” átomos de Boro e Carbono em armadilhas de íons, e quando expostos à pressão e temperatura controlados, os componentes se arranjaram em moléculas com triplas ligações. Desse resultado esplêndido, algumas considerações podem ser feitas, segundo o grupo de estudo.
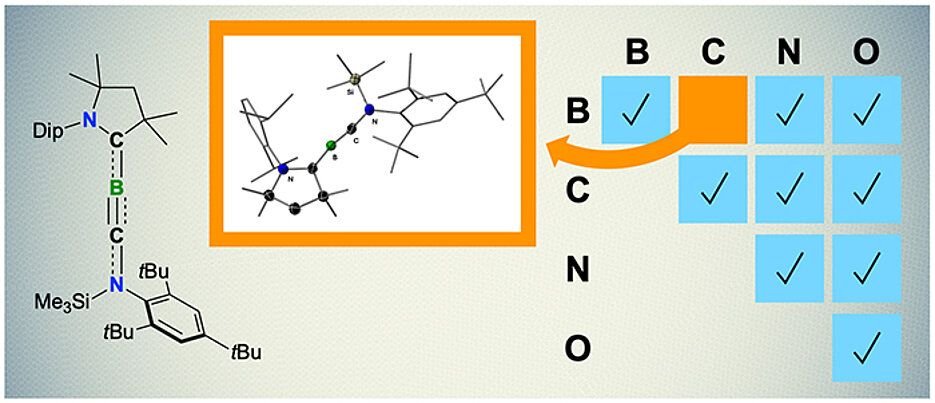
Observou-se, por exemplo, que ainda que a molécula, chamada então de Borino, seja real e possível de ser formada, o Boro fica “desconfortável” em uma ligação linear com o carbono. Todos os átomos possuem ângulos ideias de ligação, mesmo que alguns sejam mais “flexíveis” as ligações produzidas em angulações muito extremas podem ser frágeis. Isso confere reatividade a essas moléculas.
Em um exemplo banal, é como aquela mesa que você insistiu em montar sem as instruções e sem as ferramentas adequadas. Ela está em pé, porém se alguém se aproximar, corre o risco dela desmontar completamente.

Mas coisas que “quebram fácil” podem ser muito úteis, por isso, os novos passos da pesquisa serão em direção à compreensão de como essa tripla ligação pode se manter estável e quais são os impactos da reação de quebra dessas moléculas.
No Tetris molecular, ângulos e reações são essenciais para o desenvolvimento de moléculas úteis para o desenvolvimento de novas medicações, assim como para produção de energia e armazenamento de energia.
Naturalmente, esse tipo de ligação entre o Boro e o Carbono podem não ter sido detectadas anteriormente, devido à necessidade de controle de pressão e temperatura para manter estável a posição do Boro. Quem diria que elementos da Tabela Periódica também podem ter dor nas costas?
O grupo de pesquisa ainda faz uma reflexão sobre a importância das pesquisas “aparentemente” banais, citando descobertas que contribuíram de diferentes maneiras no cotidiano, como o desenvolvimento do teflon e da supercola.

O avanço da tecnologia está intimamente atrelado às observações que fazemos no cotidiano, seja no laboratório ou na mistura correta de ingredientes. Conhecer como os elementos funcionam, se ligam e desfazem suas ligações químicas contribuem para que seus usos possam ser generalizados ou assumir novas funções.
O Ozempic, por exemplo, é uma medicação produzida inicialmente para o controle da diabetes, contudo, o mecanismo de ação das moléculas presentes na medicação, também induzem efeitos fisiológicos que contribuíram para o tratamento de perda de peso.
Assim, ainda não sabemos quais são os potenciais para as moléculas de tripla ligação entre Boro e Carbono, porém, essa tentativa inédita pode futuramente trazer resultados interessantes para o desenvolvimento de novas tecnologias.
Enquanto esperamos novidades, conheça um pouco mais sobre a Tabela Periódica, começando pelo elemento que compõe 78% da nossa atmosfera: o nitrogênio! Para mais novidades, continue acompanhando o TecMundo e nos conte em nossas redes o que mais você gostaria de saber sobre a Ciência, a vida e o Universo! Até mais.

